Anvisa encerra análise para uso da vacina da CanSino
Houve um desacordo entre fabricante chinesa e representante no Brasil

A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou, na noite dessa segunda-feira (28), que encerrou o processo de análise da autorização temporária de uso emergencial, em caráter experimental, da vacina chinesa da CanSino. A decisão tomada, por unanimidade, pela diretoria colegiado do órgão após um desacordo entre a fabricante chinesa e sua representante no Brasil.
Em nota, a Anvisa explicou que o processo foi encerrado "sem a continuidade da avaliação de mérito do pedido", que foi feito pela então representante do imunizante no país, a Convidecia, no dia 18 de maio de 2021.
Ainda segundo a linha do tempo detalhada pela Anvisa, a Gerência Geral de Medicamentos e Produtos Biológicos da agência foi notificada por e-mail, no dia 17 de junho de 2021, pela CanSino Biologics Inc., que a Belcher Farmacêutica e o Instituto Vital Brazil S.A. não possuíam mais autorização para representar a empresa no Brasil.
No dia 18 de junho, a Anvisa informou o Ministério da Saúde sobre o comunicado da CanSino Biologics. No dia 21, diretores da agência se reuniram com representantes da Belcher, que afirmaram que a situação era um "dissenso comercial" e solicitaram um prazo para se manifestar sobre o caso. Já no dia 22 de junho, também segundo a agência, a Belcher confirmou a revogação do contrato de representação da CanSino. Já no dia 27, a farmacêutica chinesa ratificou que a companhia brasileira não era mais sua representante.
"A perda de legitimidade processual da empresa Belcher Farmacêutica do Brasil Ltda e do Instituto Vital Brazil S.A. para atuar perante esta agência por autorização da empresa CanSino Biologics Inc. enseja a ausência de condições para manutenção da continuidade da avaliação do pedido de autorização de uso emergencial da vacina Convidecia perante a Anvisa. Aplica-se, ao caso, o disposto no inciso I do art. 9º da Lei nº 9.784/99, por perda de legitimidade da empresa Belcher Farmacêutica do Brasil Ltda e do Instituto Vital Brazil S.A. para atuarem interessados no presente processo administrativo", ressaltou a nota da Anvisa.
A CanSino solicitou a substituição do seu representante nacional, mas, para a Anvisa, a "ação não se figura como alternativa administrativamente viável". Um novo pedido de análise deverá ser protocolado para que a vacina seja analisada pela agência.
A Anvisa explicou que a Belcher também pode solicitar nova análise da vacina, "desde que sanada a contestação de representação junto ao fabricante".
A vacina Convidecia, fabricada pela empresa CanSino Biologics Inc., localizada na China, atualmente está aprovada para uso em oito países: Argentina, Chile, China, Equador, Hungria, Malásia, México e Paquistão.
 Medida Ministério da Saúde começa distribuição emergencial de medicamento oncológico no Brasil
Medida Ministério da Saúde começa distribuição emergencial de medicamento oncológico no Brasil 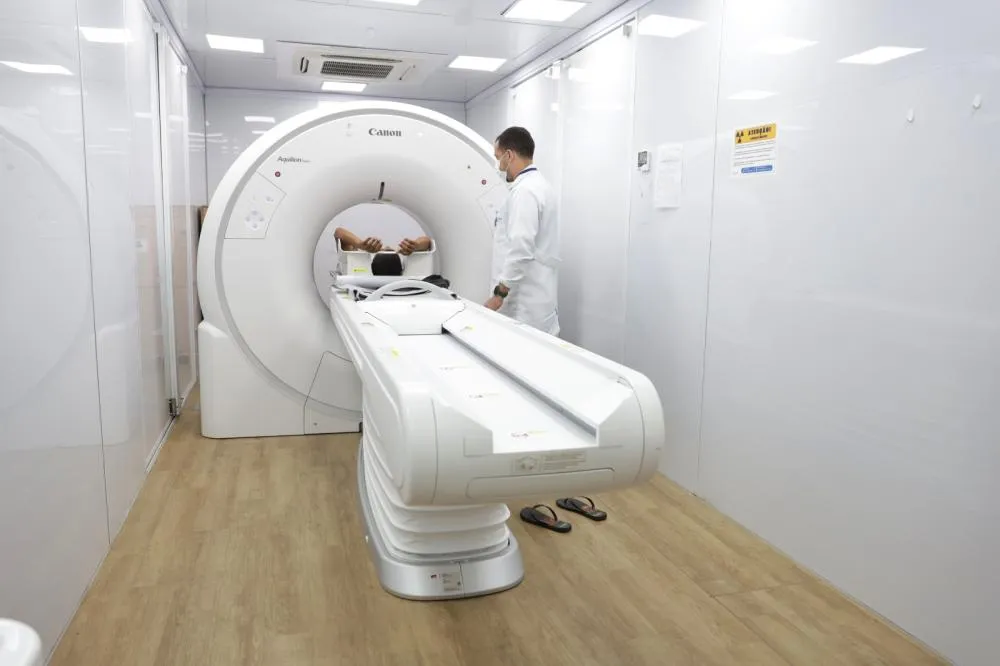 Saúde Bahia e Brasil ampliam parceria na saúde com anúncio de R$ 66,49 milhões para 34 municípios
Saúde Bahia e Brasil ampliam parceria na saúde com anúncio de R$ 66,49 milhões para 34 municípios 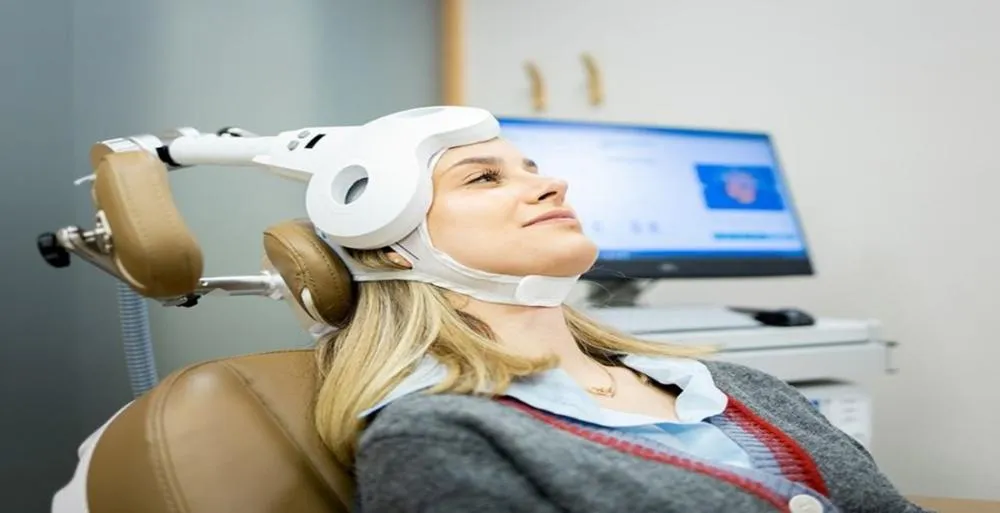 Neuromodulação Neuromodulação ganha espaço no tratamento da dor crônica e do estresse
Neuromodulação Neuromodulação ganha espaço no tratamento da dor crônica e do estresse  Saúde Santa Casa de Cachoeira é reativada com novos serviços e investimento milionário nas comemorações do seu bicentenário
Saúde Santa Casa de Cachoeira é reativada com novos serviços e investimento milionário nas comemorações do seu bicentenário  Palavra de médico O “Palavra de Médico” deste domingo falou sobre os desafios da saúde mental
Palavra de médico O “Palavra de Médico” deste domingo falou sobre os desafios da saúde mental  Alzheimer Novo medicamento contra Alzheimer deve chegar ao Brasil em junho
Alzheimer Novo medicamento contra Alzheimer deve chegar ao Brasil em junho 
Mín. 21° Máx. 31°
Mín. 21° Máx. 31°
Chuvas esparsasMín. 20° Máx. 32°
Tempo nublado





